«Чтобы у пациента было время ждать»: специалист-онколог — о методиках иммунотерапии рака
Специалист НМИЦ им. Н.Н. Блохина рассказал об иммунотерапии рака
- Gettyimages.ru
- © gorodenkoff
— Выступая на ПМЭФ, министр здравоохранения России Михаил Мурашко сообщил, что первые результаты доклинических исследований российской вакцины против рака могут быть представлены уже в конце 2024 года. Разработкой препарата занимается НМИЦ онкологии им. Н.Н. Блохина и НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи. Расскажите, пожалуйста, о разрабатываемом препарате. Против каких видов рака он будет работать?
— Идея такой вакцины появилась на фоне пандемии коронавируса, когда для профилактики COVID-19 стали создаваться РНК-вакцины. Такая технология позволяет быстро создавать препараты для иммунизации людей против определённого антигена. Вакцины оказались достаточно эффективными, стимулировали выработку нужного объёма антител. Это натолкнуло учёных на идею создания по аналогичному принципу вакцины против злокачественных опухолей. Сложность тут в том, что если у вируса есть несколько всегда повторяющихся антигенов, то опухоли очень индивидуальны, их антигены сильно отличаются у разных пациентов.
В нашем институте как раз велась в то время разработка так называемых неоантигенных вакцин. Для этого мы изучали состав антигенов разных видов рака, в первую очередь меланомы, поскольку этот вид рака хорошо поддаётся иммунотерапии. В итоге мы объединили усилия с коллегами из центра им. Н.Ф. Гамалеи, чтобы создать РНК-вакцину против рецидива рака кожи. Антигены клеток меланомы сильно отличаются от нормальных белков и могут быть замечены иммунитетом. Эти белковые последовательности можно перевести в цепочку РНК: попадая в организм, она будет провоцировать иммунный ответ и учить иммунитет распознавать и атаковать такие же комбинации белков. И соответственно, уничтожать опухоль. В данном случае можно препарат делать индивидуально под конкретного пациента. Именно над разработкой такого препарата мы сейчас и работаем.
- Раковая опухоль
- Gettyimages.ru
- © SCIEPRO SCIENCE / PHOTO LIBRARY
— Ранее группа иностранных учёных тоже разработала новые рекомбинантные антитела, способные активировать работу иммунной системы против клеток светлоклеточного рака почки. Расскажите, пожалуйста, по какому принципу работает метод, описанный иностранными учёными, и в чём его отличие от других?
— В данном случаеречь идёт о так называемых неспецифических антителах, которые могут облегчать взаимодействие между опухолевыми клетками и иммунными клетками пациента, которые в естественных условиях на это не способны. Новый класс антител позволяет механически сблизить Т-клетки и опухолевые клетки. Благодаря этому Т-клетки начинают выполнять свою работу, разрушая опухоль.
 «Стражи генома»: российские онкологи — о причинах раннего развития рака и методиках лечения
«Стражи генома»: российские онкологи — о причинах раннего развития рака и методиках лечения
— Именно способность раковых клеток прятаться от иммунной системы является главной проблемой в случае рака. Все ли виды рака маскируются от иммунитета? За счёт чего раковым клеткам удаётся уходить от иммунного ответа?
— Да, верно, способность раковых клеток прятаться от иммунной системы — это серьёзная проблема. Дело в том, что все наши органы и системы в ходе эволюции оттачивались под определённые задачи. Иммунная система не была эволюционно приспособлена для уничтожения раковых клеток по одной простой причине: онкологические заболевания, как правило, развиваются уже в пострепродуктивном возрасте, когда передать потомству какие-то признаки уже нельзя. Так что это не опухоль такая хитрая и умело прячется, а наша иммунная система не научена её распознавать. Тем более что белки раковых клеток очень похожи на белки здоровых клеток, а иммунная система заточена под распознавание совсем чужеродных антигенов — белков инфекционных возбудителей, вирусов и бактерий.
- Т-клетки иммунитета
- Gettyimages.ru
- © JUAN GAERTNER / SCIENCE PHOTO LIBRARY
Тем не менее иммунная система всё же отчасти следит за появлением злокачественных клеток и уничтожает их, то есть осуществляет иммунный надзор. Впервые это ещё в 1960-х годах предположил австралийский вирусолог-иммунолог Фрэнк Макфарлейн Бёрнет, нобелевский лауреат по медицине.
К счастью, наука развивается, она уже многое знает о том, как устроена иммунная система. Эти знания позволяют нам учить иммунные клетки распознавать белки на поверхности опухолевых клеток и уничтожать их.
 Препараты индивидуального действия: российские учёные разработали новый подход к созданию противораковых вакцин
Препараты индивидуального действия: российские учёные разработали новый подход к созданию противораковых вакцин
— Раковые клетки становятся «невидимками» с самых первых моментов или уже на более поздних стадиях, когда образуется опухоль? Может ли хороший иммунитет помочь в профилактике рака?
— Этот вопрос часто задают наши пациенты: я заболел, потому что у меня плохой иммунитет? Это не так. Надо понимать, что разные виды рака возникают по разным причинам, сегодня все они более-менее известны. При этом процесс формирования опухоли всё равно схож у всех видов рака: сначала нормальная клетка мутирует, начинает бесконтрольно делиться, через поколения таких мутировавших клеток формируются уже опухоль и метастазы. А причины у изначальной мутации могут быть разными — например, в случае рака шейки матки канцерогенным фактором является вирус папилломы человека (ВПЧ). Вирус повреждает клетки покровного эпителия, они становятся злокачественными. И этот вид рака можно предотвратить, если не допустить размножение данного вируса в организме.
Другой пример канцерогенного фактора — курение. Под воздействием смол, канцерогенов, которые содержатся в табачном дыме, в клетках возникают множественные повреждения ДНК и РНК. Так возникают соматические (клеточные) мутации, в клетках появляются видоизменённые белки, опухолевые антигены, или неоантигены. На этом этапе это ещё может быть не злокачественная опухоль, а предраковое состояние.
— Возвращаясь к теме иммунотерапии рака: какие её виды существуют? Бывает ли, что иммунная система сама, естественным образом замечает опухоль и начинает с ней бороться?
— Сегодня считается, что есть виды опухолей, которые иммунная система способна распознать. Однако в ответ опухоли запускают молекулярные механизмы, которые гасят уже начавшуюся в организме иммунную реакцию. Этот механизм иначе называется системой иммунных контрольных точек (ИКТ, англ. Immunological checkpoints). Совсем недавно по меркам науки учёные научились блокировать эти контрольные точки, что позволяет иммунной системе работать против опухоли в полную силу. Благодаря этому стало возможно лечить многие виды рака.

- Курение
- Gettyimages.ru
- © JGI / Tom Grill
Есть и другой вариант, когда опухоль не блокирует иммунный ответ, а просто её белки настолько похожи на нормальные, что иммунитет не в состоянии их распознать. В этом случае иммунный ответ с самого начала невозможен. Тогда требуется уже применение иммунных препаратов, которые содержат иммунные агенты, модифицированные таким образом, чтобы они могли атаковать опухоль. Это, например, технология CAR-T. В этом случае у пациента забирается часть лимфоцитов, в клеточной лаборатории они специальным образом перепрограммируются под конкретную мишень — опухоль этого пациента. Это весьма сложный процесс.
 «Нарушения в их работе могут спровоцировать онкологию»: биолог — о роли митохондрий клетки
«Нарушения в их работе могут спровоцировать онкологию»: биолог — о роли митохондрий клетки
Есть более простая технология создания биспецифических антител, то есть способных атаковать сразу две мишени, два разных белка. Такие антитела можно разрабатывать под любые мишени и производить в промышленных количествах. Механизм работы таких препаратов следующий: биспецифическое антитело как бы связывает раковую клетку с лимфоцитами, выступает мостом между иммунной системой и опухолью. Сблизившись с раковой клеткой, лимфоцит уже начинает её распознавать и уничтожать.
— Какие есть противопоказания для иммунотерапии?
— В данном случае мне не очень нравится термин «противопоказания». Речь скорее идёт об оценке рисков и о целесообразности. В случае иммунотерапии основной риск — гиперреактивность иммунной системы, так называемый цитокиновый шторм. Тормозящие иммунный ответмеханизмы, о которых я говорил ранее, в норме нужны организму, чтобы иммунная система не атаковала собственные ткани и органы. И когда мы его отключаем, есть риск, что иммунитет начнёт поражать не только опухоль, но и здоровые системы организма, то есть начнётся аутоиммунная реакция. В случае с биспецифическими антителами такой риск меньше, потому что они нацелены всё же на конкретные мишени, расположенные именно на опухолевых клетках.
К сожалению, иммунотерапия — это не живая вода, которая может поднять на ноги уже умирающего пациента. Чтобы она сработала, нужно, чтобы в организме было достаточное количество иммунных клеток — больше, чем опухолевых.
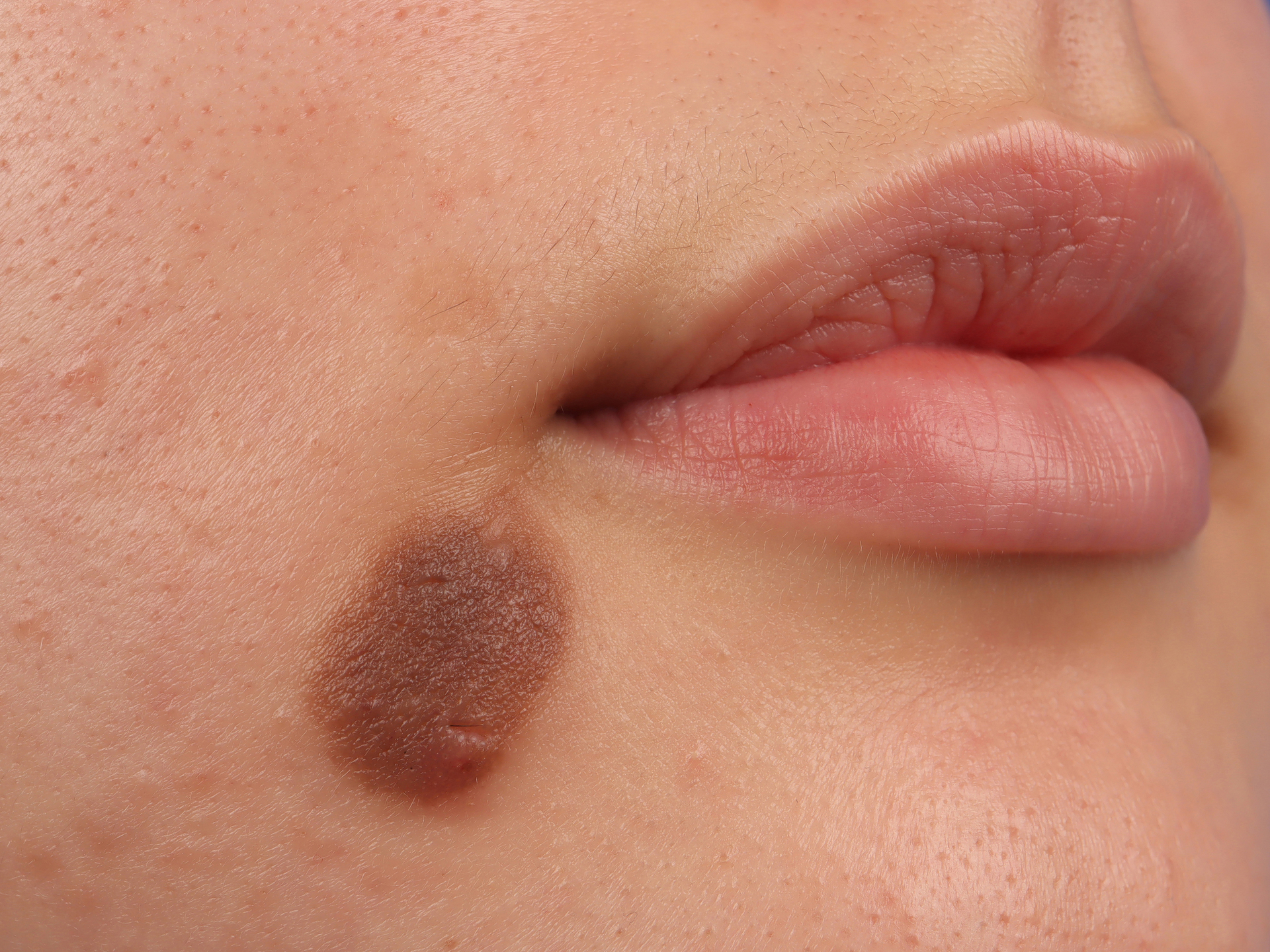
- Меланома
- Gettyimages.ru
- © GIRAND / BSIP / Universal Images
— Какова эффективность иммунотерапии для разных типов рака? И какие результаты она показывает на пациентах, а не в лабораторных условиях?
— Это отнюдь не праздный вопрос. Изначально, когда иммунотерапия только разрабатывалась, была эйфория и надежды, что она позволит покончить с раком. Однако сейчас уже накоплены данные, которые позволяют оценить её реальную эффективность. Есть виды рака, которые очень хорошо реагируют на такую терапию — например, против лимфом эффективность может достигать 90%. Дело в том, что провоцирующий лимфомы вирус Эпштейна — Барр создаёт такие хромосомные нарушения в клетках, которые становятся очень заметной мишенью для терапии.
 «Запускается целый каскад изменений»: нейробиолог — о последствиях и профилактике хронического стресса
«Запускается целый каскад изменений»: нейробиолог — о последствиях и профилактике хронического стресса
Также иммунотерапия эффективна примерно для трети пациентов с меланомой — и это хороший результат для этого агрессивного рака. Этот список можно продолжать долго, для больных каждым видом рака иммунотерапия стала дополнительным шансом. Однако на 100% решить проблему онкологии она не позволяет, как и все другие методики. Что касается того, на какой стадии рака она помогает, то тут стандартная классификация стадий не играет очень большой роли, важнее общий объём раковых клеток и наличие на них потенциально заметных для иммунной системы антигенов. Кроме того, важно, чтобы все остальные системы организма работали нормально, чтобы у пациента было время ждать, пока иммунная терапия сработает.
— Производятся ли препараты для иммунотерапии рака в России?
— Да, есть, например, производители блокаторов иммунного ответа, о которых я говорил в начале, этим направлением занимается несколько компаний. Уже есть отечественные иммунотерапевтические препараты с хорошей эффективностью. В том числе инновационные, не являющиеся копиями иностранных разработок. И такая терапия достаточно широко применяется в России. Проводится также клеточная терапия CAR-T. Пока что хуже дело обстоит с биспецифическими антителами, поскольку это достаточно новая технология. Однако это очень перспективное направление.
- «Подойдёт для длительного лечения»: разработчик — о новом российском препарате от болезни Бехтерева
- «Клетка в клетке»: российские учёные выявили способность энтоза влиять на развитие онкологии
- «Смысла в радикальных диетах нет»: завкафедрой общей врачебной практики РУДН — о новых методиках лечения атеросклероза
- «Нет ничего вреднее, чем сахар»: российский стоматолог — о заболеваниях зубов и передовых методиках лечения
- «Наиболее часто встречающаяся причина деменции»: профессор — о симптомах и методах профилактики болезни Альцгеймера
- «Один из самых сильных природных ядов»: специалисты — о проявлениях и профилактике ботулизма